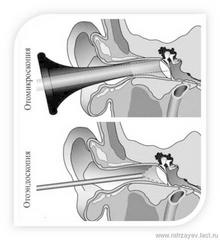
Внедрение современной эндоскопической технологии в клиническую оториноларингологию за последние десятилетия, позволило значительно расширить практические возможности эндоскопических операций при некоторых заболеваниях уха, и тем самым способствовало развитию приоритетного направления – эндоскопической отохирургии.
Актуальность использования эндоскопических методов в отохирургии во многом определяется возможностью получения оптимальной визуализации с увеличением изображений анатомических структур среднего и внутреннего уха, недостаточно обозримых при прямой микроскопии через операционный микроскоп, а также проведения качественной элиминации очагов поражения из областей, являющихся труднодоступными при выполнении отомикрохирургической операции (ОМО).
В настоящее время, отоэндоскопические операции (ОЭО) проводятся при некоторых гнойных и негнойных заболеваниях уха. Применение эндоскопов позволяет провести полипроекционный осмотр ряда «скрытых зон» операционного поля, недостаточно визуализирующийся при ОМО: переднее эпитимпанальное пространство, медиальные синусы ретротимпанума, глубокие отделы гипотимпанума, ретрофациальный отдел сосцевидной полости, овальное и круглое окна.
Среди хронических гнойных средних отитов (ХГСО), ОЭО наиболее часто применяются при мезо – и эпитимпанитах, осложненных холестеатомой [1-8], а также при сухих перфорациях барабанной перепонки (БП) [6,9-15].
В зависимости от локализации и распространенности патологического очага в ухе, ОЭО применяется либо как самостоятельный хирургический метод, либо – в комбинации с ОМО в качестве эндоскопической ассистенции.
Как самостоятельный хирургический метод, ОЭО чаще проводятся при «аттикальной» (ограниченной) холестеатоме СУ [1-8]. При данной патологии операция выполняется путём эндомеатального подхода, зачастую с использованием эндоскопов с углом зрения 0°, 30° и 45° оптики. Основным преимуществом ОЭО, по мнению исследователей, является особенности устройства эндоскопа, позволяющий под благоприятным углом зрения осмотреть ряд труднодоступных структур (трудно визуализируемые вовремя ОМО) расположенных в ретротимпанальном и переднем эпитимпанальном пространствах СУ. Использование эндоскопов при этом упрощает технику выполнения ряда операций, считавшиеся трудновыполнимыми при традиционном методе оперирования.
В качестве самостоятельного метода, ОЭО также широко применяются как при первичной, так и резидуальной и/или рецидивирующей холестеатоме СУ [1-8]. Наряду с известными преимуществами эндоскопов при выполнении ОЭО, констатированы и другие отличительные особенности, которые позволяют из разных угловых плоскостей, визуализировать ряд «скрытых зон» (расположенных под большим углом зрения) в анатомически сложной и узкой полости СУ.
Известно, что одним из причин неблагоприятного исхода хирургического лечения больных с приобретенными холестеатомами СУ является рецидив холестеатомы. Наиболее часто рецидивы возникают в случаях неполного удаления холестеатомного матрикса, сохранение которого приводит к развитию повторной ретракции БП [16]. С одной стороны, этому способствует топографо-анатомическая особенность строения СУ, включающая в себе ряд труднодоступные для полноценной визуализации (во время операции) отделы, с другой – стремление хирурга к максимальному сохранению целостности функционирующих структур, расположенных в очаге поражения. В тоже время, малоинвазивные хирургические вмешательства, проводимые путём ОЭО, в силу обеспечения адекватной элиминации патологического очага из «скрытых зон» операционного поля, могут претендовать на некоторые преимущества перед ОМО. Одним из недостатков операционного микроскопа при этом является ограничение возможности обеспечения линейного поле зрения глубоких и боковых карманов СУ, которые не всегда рассматриваются в полном объеме.
При наличии распространяющиеся холестеатоме СУ, некоторые авторы, предпочитают комбинировать ОМО, эндоскопической ассистенцией [1-8]. Использование операционного микроскопа при этом, чаще всего возникает в случаях необходимости работать двумя руками: при удалении холестеатомного матрикса и/или стелющегося эпидермиса с тимпанального сегмента ЛН, со слуховых косточек, с подножной пластинки стремени, а также при реконструкции цепи слуховых косточек.
Роль эндоскопической ассистенции, при выполнении комбинированной операции, заключается в отоэндоскопической ревизии трепанационной полости и/или санации необнаруженных во время ОМО патологических очагов, как на отдельных, так и завершающих этапах санирующей операции на ухе [4,5,18-21]. Так, по данным D. Biswas с соавт. [22], в числе больных, подвергшихся санирующей операции, отоэндоскопия, проведённая на завершающем этапе операции, позволила обнаружить резидуальную холестеатому (в тимпанальной части трепанационной полости) в 12,5% случаев, наличие которой не удалось выявить во время ОМО. Проведённая, в качестве эндоскопической ассистенции, ОЭО, во всех случаях, обеспечила полное удаление холестеатомы – рецидивы заболевания при динамическом наблюдении за пациентами (в сроках до 6 месяцев) не выявлены. По мнению авторов, благодаря обеспечению панорамного обзора трепанационной полости, отоэндоскопия, позволяет визуализировать резидуельные холестеатомы, находящиеся в областях, труднообозримых при выполнении ОМО.
Сравнительная оценка эффективности применения традиционного метода хирургического вмешательства и эндоскопической технологии у пациентов с холестеатомой СУ (на основе анализа и обобщения литературных данных), позволила L. Presutti с соавт. [23], констатировать факт преимущества применения ОЭО (как в качестве самостоятельного метода, так и в комбинации с ОМО) по сравнению с ОМО, выполненной традиционным методом. Так, в числе оперированных больных (515 больных или 517 операций) в 293 (57%) случаях была выполнена исключительно ОЭО, и 224 (43%) – проведена комбинированная (ОМО+ОЭО) операция. В послеоперационном периоде, резидуальная холестеатома или рецидивы заболевания были обнаружены у 48(9,3%) больных. Сопоставление полученных данных, с данными, частоты выявления таковых (20-30%) у оперированных традиционным методом больных, позволило автором обосновать преимущества ОЭО над ОМО, не только в отношении качества выполняемой операции, но и – принципа малоинвазивности хирургического вмешательства.
Отмечая успешное применение эндоскопов в отохирургии, ряд авторов, вместе с тем, указывают на эффективность санации патологических очагов трепанационной полости при использовании эндоскопа [24]. Так, отоэндоскопия, в большинстве случаев (61,1%), позволяет качественно проводить санацию патологических очагов (грануляций, рубцовых мембран, кист), образованных после «открытых» типов санирующих операций на среднем ухе, по сравнению с таковой, проводимой под микроскопом (21,4%). По мнению авторов, эндоскопическая санация трепанационной полости, наряду с применением традиционных методов, может в значительной степени улучшить результаты лечения больных с так называемой «болезнью оперированного уха».
Как самостоятельный метод, ОЭО получила распространение также при перфорации БП [6,9-15]. Данная операция особенно оправдывается при краевой перфорации в переде-верхнем квадранте БП [14,25], ибо применение традиционной операции при некоторых обстоятельствах чревато рядом сложностей. Одним из таких обстоятельств является анатомическая особенность НСП, характеризующаяся наличием косого расположения его костного отдела, в дистальной части которого, верхние квадранты БП располагаются более наклонно. Из-за ограничения разрешающей способности операционного микроскопа при этом, угловое обозрение БП затрудняется, что нередко является причиной проведения дополнительных вмешательств – выполнение заушного разреза и расширение просвета НСП, несмотря даже на изменения расположения головы пациента и/или положения микроскопа [15]. Между тем, эндоскопическая мирингопластика, в силу разрешающей способности эндоскопа (обеспечивающий панорамный обзор структур СУ), лишена указанных недостатков, и независимо от размера и/или места расположения перфорации, практически во всех случаях позволяет произвести радикальную коррекцию БП [15]. При этом качественная пластика БП, во многом зависит от подготовки достаточно широкой ложи для трансплантата, реализация, которой достигается при помощи эндоскопа, обеспечивающего благоприятные углы поля зрения, особенно передне-верхнего и/или передне-нижнего квадрантов БП [21,26].
Следует отметить, что применяя ОЭО в качестве самостоятельного метода при субтотальных и тотальных перфорациях БП, некоторые авторы нередко комбинируют данный метод с ОМО [6,9-15]. Применение последней в качестве отомикрохирургического ассистирования (видоизмененная комбинированная операция), по мнению большинства исследователей, является высокоэффективным методом, который позволяет в подавляющем большинстве случаев (от 80 до 100%) восстановить целостности БП.
В течение последнего десятилетия ОЭО, как метод выбора нашла свое применение также при некоторых негнойных заболеваниях уха, в частности при отосклерозе [19,21,27,28] и кохлеарной имплантации (КИ) [29-32]. Эффективность ОЭО, по мнению большинства её сторонников, обусловлена оказанием малоинвазивного вмешательства, позволяющего предотвратить возможных повреждений барабанной струны (БС) и ЛН.
Так, традиционная стапедоплдастика, в зависимости от анатомической вариабельности, формы, строения и размеров НСП, а также структур СУ (наличие атипичного хода ЛН, значительное нависание ЛН над окном преддверия, выпячивание ЛН в нишу окна преддверия возникшее вследствие дефекта костной стенки фаллопиева канала), может оказаться технически трудновыполнимой. В то же время для улучшения обзора структур заднего тимпанального отдела – стремени, пирамидального отростка, канала ЛН и длинной ножкой наковальни нередко требуется удаление заднего края, выступающей кости задне-верхней стенки НСП (annulus tympanicus). Чрезмерное удаление annulus tympanicus, в свою очередь создает угрозу развития травматического вывиха наковальни [33-35], для устранения которого, зачастую требуется реоперация. Последняя, в силу ряда обстоятельств, является трудновыполнимым и травматичным вмешательством.
Что касается возможных осложнений, связанных с повреждением БС, следует отметить, что при её травме во время операции в большинстве случаев (20-60%) после стапедопластики возникает нарушение вкуса (на передних двух третей языка) или выпадение функции слюноотделения [33-38]. Следовательно, сохранность БС имеет существенное значение особенно при двусторонней стапедопластике [37,39,41,42], ибо двустороннее повреждение её может привести к временному, либо постоянному выпадению функции БС. В результате полного угнетения функции слюноотделения развиваются такие необратимые патологические процессы, как ксеростомия (повышение сухости слизистой оболочки полости рта) и/или осязательная дисгевзия [42-44] со всеми вытекающими последствиями: ощущение постоянного устойчивого металлического (или кислого) вкуса и чувство жжения во рту.
Несмотря на возможности операционного микроскопа обеспечивающего трехмерного изображения структур в анатомически узкой полости СУ, эндоскопическая стапедопластика в силу известных разрешающих способностей эндоскопа, имеет рад преимуществ перед традиционно выполненной операцией. Исходя из отличительных особенностей эндоскопа, эндоскопическая стапедопластика, в настоящее время широко применяется в качестве самостоятельной операции, которая наряду с достижением эффективного лечения, обеспечивает также и безопасность хирургического вмешательства [27-29].
В настоящее время КИ (с системой реабилитационных мероприятий) остается единственным методом, позволяющим у большинства глухих людей, обеспечить частичное или полное восстановление слуха. Операция проводится при помощи операционного микроскопа путём реализации стандартной мастоидотомии и задней тимпанотомии, выполнение которых обеспечивает доступ к полости СУ и круглому окну. Между тем, несмотря на разрешающие способности микроскопа, из-за ограничения его возможности в обеспечение линейного поля зрения круглого окна (угол обзора, меньше чем хотелось бы), не удается визуализировать её нишу в полном объёме. При этом создаются определенные трудности, связанные с наложением кохлеостомы (вскрытие внутреннего уха) предназначенной для введения активного электрода. В тоже время попытки реализации широкой задней тимпанотомии (более 2 мм) произведенной под микроскопом, из-за известных ограничений, имеющих место в его разрешающей способности, чреваты повреждением цепи слуховых косточек, БС, ЛН и/или БП.
Разработка и внедрение в практику КИ супрамеатального доступа [45], позволило устранить необходимость проведения традиционной мастоидотомии и задней тимпанотомии, а также устранить угрозу повреждения структур среднего и/или внутреннего уха. Широкое применение модифицированной КИ (с использованием данного доступа) в практику, значительно улучшило результаты КИ у оперированных больных [31,46-51]. Модифицированная КИ, осуществляемая путём реализации эндоскопической тимпанотомии и мембранной кохлеостомы, позволяет осуществить беспрепятственное введение электродов (после эндоскопической тимпанотомии) в барабанную лестницу улитки (sacula tympani), непосредственно через мембрану круглого окна (мембранная кохлеостома), обеспечивая при этом безопасности хирургического вмешательства.
Отмечая положительные качества ОЭО, следует иметь в виду также и некоторые правила, нарушение которых, могут привести к осложнениям при работе с эндоскопами, особенно при использовании эндомеатального подхода. Так, при недостаточности навыков работы с эндоскопами, осложнение могут возникнуть вследствие травмы ЛН, цепи слуховых косточек, и интактной крыши барабанной полости (tegmen tympani), непосредственно в результате касания дистального конца эндоскопа в эти структуры. Знание особенностей эндоскопической анатомии СУ, а также развитие необходимой зрительно-моторной координации при работе с эндоскопами в анатомически узкой полости СУ, могут устранить указанные погрешности и способствовать успешному исходу операции [52].
Несмотря на огромные успехи, достигнутые в области эндоскопической хирургии носа, околоносовых пазух и основания черепа за последние десятилетия, внедрение эндоскопической технологии в клиническую практику отиатрии, по настоящее время не нашло свое широкое развитие в сете национальных практических и научно-исследовательских медицинских учреждений России и стран СНГ. Разработка проекта по внедрению ОЭО в клиническую практику, формирование концептуальных позиций, накопление первоначального опыта и определение спектра возможного клинического применения, позволят в значительной степени оценить достоинства отоэндоскопической хирургии при различных заболеваниях уха.
ЛИТЕРАТУРА
- Tarabichi M. Endoscopic middle ear surgery. Ann Otol Rhinol Laryngol. 1999; 108:39-46. htths://doi org/10.1177/00034894991080010
- Yung MW. The use of middle ear endoscopy: has residual cholesteatoma been eliminated? J Laryngol Otol. 2001; 115:958-961. htths://doi org/10.1258/0022215011909765
- El-Meselaty K, Badr-El-Dine M, Mandour M, Maurad M, Darweesh R. Endoscope affects decision making in cholesteatoma surgery. Otolaryngol Head Neck Surg. 2003; 129:490-496. htths://doi org/10.1016/s0194-5998(03)01577-8
- Tarabichi M. Endoscopic management of limited attic cholesteatoma. 2004; 114:1157-1162. htths://doi org/10.1097/00005537-200407000-00005
- Barakate M, Bottrill I. Combined approach tympanoplasty for cholesteatoma: impact of middle-ear endoscopy. J Laryngol Otol. 2008; 122:120-12. htths://doi org/10.1017/s0022215107009346
- Mohindra S, Panda NK. Ear surgery without microscope; is it possible. Indian J Otolaryngol Head Neck Surg. 2010; 62:138-141. htths://doi org/10.1007/s12070-010-0033-5
- Wilson KF, Hoggan RN, Shelton C. Tympanoplasty with intact canal wall mastoidectomy for cholesteatoma: long-term surgical outcomes. Otolaryngol Head Neck Surg. 2013; 149:292-295. htths://doi org/10.1177/0194599813489521
- Tomlin J, Chang D, McCutcheon B, Harris J. Surgical technique and recurrence in cholesteatoma: a meta-analysis. Audiol Neurootol. 2013; 18:135-142. htths://doi org/10.1159/000346140
- Usami S, Iijima N, Fujita S, Takumi Y. Endoscopic-assisted myringoplasty. ORL J Otorhinolaryngol Relat Spec. 2001; 63:287-290. htths://doi org/10.1159/000055759
- Karhuketo TS, Ilomäki JH, Puhakka HJ. Tympanoscope-assisted myringoplasty. ORL J Otorhinolaryngol Relat Spec. 2001; 63:353-358. htths://doi org/10.1159/000055773
- Raj A, Meher R. Endoscopic transcanal myringoplasty-A study. Indian J Otolaryngol Head Neck Surg. 2001; 53:47-49. htths://goi org/10.1007/bf02910979
- Yadav SP, Aggarwal N, Julaha M, Goel A. Endoscope-assisted myringoplasty. Singapore Med J. 2009; 50:510-512. htths://doi htths://doi org/10.5455/jorl.51-1327835507
- Konstantinidis I, Malliari H, Tsakiropoulou E, Constantinidis J. Fat myringoplasty outcome analysis with otoendoscopy: who is the suitable patient? Otol Neurotol. 2013; 34:95-99. htths://doi org/10.1097/mao.0b013e318278c1e3
- Ayache S. Cartilaginous myringoplasty: the endoscopic transcanal procedure. Eur Arch Otorhinolaryngol. 2013; 270:853-860. htths://doi org/10.1007/s00405-012-2056-x
- Takatoshi F, Tomoo W, Tsukasa I, Toshinori K, Seiji K. Feasibility and Advantages of Transcanal Endoscopic Myringoplasty. Otology & Neurotology. 2014; 35, 140-145. htths://doi org/10.1097/mao.0000000000000298
- Kasenõmm P. Intraoperative findings in revision mastoid surgery. Acta Oto-Laryngologica.2013; 133(8):826-832. htths://doi org/10.3109/00016489.2013.787645
- Rosenberg SI, Silverstein H, Willcox TO. Endoscopy in otology and neurotology. Am J Otol. 1994; 15:168-72. htths://doi org/10.1016/s0194-5998(05)80264-5
- Youssef TF, Poe DS. Endoscope-Assisted Second-Stage Tympanomastoidectoy. 1997; 107(10):1341-1344. htths://doi org/10.1097/00005537-199710000-00009
- Poe DS. Laser-assisted endoscopic stapedectomy: a prospective study. Laryngoscope. 2000; 110 (Suppl 95):1-30. htths://doi org/10.1097/00005537-200005001-00001
- Harugop AS, Mudhol RS, Godhi RA. A comparative study of endoscope assisted myringoplasty and micrsoscope assisted myringoplasty. Indian J Otolaryngol Head Neck Surg. 2008; 60:298-302. htths://doi org/10.1007/s12070-008-0099-5
- Мисюрина Ю. В. Клинико-экспериментальное обоснование применения эндоскопической техники на отдельных этапах санирующих и слухоулучшающих операций на среднем ухе: Дис. … канд. мед. наук. Санкт-Петербург. 2010. Ссылка активна на 02.03.2018. Доступно по http://lornii.ru/resources/autoref/misjurina_uv.pdf
- Biswas D, Mandal K, Roychoudhury A, Roychowdhury R. Otoendoscopy - A New Horizon in Ear Surgery. Bengal Journal of Otolaryngology and Head Neck Surgery.2014;1(22):4-7. Ссылка активна на03.2018. Доступно по:https://bjohns.in/journal/index.php/bjohns/article/view/2/4
- Presutti L, Gioacchini FM, Alicandri-Ciufelli M, Villari D, Marchioni D. Results of endoscopic middle ear surgery for cholesteatoma treatment: a systematic review. Acta otorhinolaryngologica Italica. 2014;34:153-157. Ссылка активна на 02.03.18. Доступно по: https://ncbi.nlm.nih.gov/pmc/articles/PMC4035841/pdf/0392-100X-34-153.pdf
- Freire GSM, Sampaio ALL, Lopes RAF, Nakanishi M, de Oliveira CACP. Does ear endoscopy provide advantages in the outpatient management of open mastoidectomy cavities? PLoS ONE. 2018; 13(1): e0191712. https://doi.org/ 10.1371/journal.pone.0191712
- Hatice C, Erdal S, Derya O. Endoscopic “Push-Trough” Technique Cartilage Myringoplasty in Anterior Tympanic Membrane Perforations. Clinical and Experimental Otorhinolaryngol. 2015; 3: 224-229. htths://doi org/10.3342/ceo.2015.8.3.224
- Halim A, Borgstein J. Pediatric myringoplasty: postaural versus transmeatal approach. Int J Pediatr Otorhinolaryngol. 2009; 73:1580-1583. htths://doi org/10.1016/j.ijporl.2009.08.010
- Nogueira Júnior JF, Martins MJ, Aguiar CV, Pinheiro AI. Fully endoscopic stapes surgery (stapedotomy): technique and preliminary results. Braz J Otorhinolaryngol. 2011; 77:721-727. htths://doi org/10.1590/s1808-86942011000600008
- Migirov L, Wolf M. Endoscopic transcanal stapedotomy: how I do it. Eur Arch Otorhinolaryngol. 2013; 270:1547-1549. htths://doi org/10.1007/s00405-013-2420-5
- Jang JH, Song JJ, Yoo JC, Lee JH, Oh SH, Chang SO. An alternative procedure for cochlear implantation: transcanal approach. Acta Otolaryngol. 2012; 132:845-849. htths://doi org/10.3109/00016489.2012.667880
- Skarzynski H, Lorens A, Matusiak M, Porowski M, Skarzynski PH, James CJ. Partial deafness treatment with the nucleus straight research array cochlear implant. Audiol Neurootol. 2012; 17:82-91. htths://doi org/10.1159/000329366
- Marchioni D, Grammatica A, Alicandri-Ciufelli M, Genovese E, Presutti L. Endoscopic cochlear implant procedure. Eur Arch Otorhinolaryngol. 2014; 271:959-966. htths://doi org/:10.1007/s00405-013-2490-4
- Migirov L, Shapira Y, Wolf M. The feasibility of endoscopic transcanal approach for insertion of various cochlear electrodes: a pilot study. Eur Arch Otorhinolaryngol. 2015; 272(7):1637-1641. htths://doi org/10.1007/s00405-014-2995-5
- Lesinski SG. Causes of conductive hearing loss after stapedectomy or stapedotomy: a prospective study of 279 consecutive surgical revisions. Otol Neurotol. 2002; 23:281-288. htths://doi org/10.1097/00129492-200205000-00009
- Szymański M, Gołąbek W, Morshed K, Siwiec H. The Influence of the Sequence of Surgical Steps on Complications Rate in Stapedotomy. Otol Neurotol. 2007; 28 (2):152-156. htths://doi org/10.1097/01.mao.0000247815.23948.89
- Malafronte G, Filosa B. Fisch's reversal steps stapedotomy: when to use it? Otol Neurotol. 2009; 30:1128-113. htths://doi org/10.1097/mao.0b013e3181be686e
- Saito T, Manabe Y, Shibamori Y, Yamagishi T, Igawa H, Tokuriki M, FukuokaY, Noda I, OhtsuboT, SaitoH. Long-term follow-up results of electrogustometry and subjective taste disorder after middle ear surgery. 2001; 111(11):2064-2070. htths://doi org/10.1097/00005537-200111000-00037
- Clark MP, O'Malley S. Chorda tympani nerve function after middle ear surgery. Otol Neurotol. 2007; 28:335-340. htths://doi org/10.1097/01.mao.0000247820.16325.f0
- Michael P, Raut V. Chorda tympani injury: operative findings and postoperative symptoms. Otolaryngol Head Neck Surg. 2007; 136:978-981. htths://doi org/10.1016/j.otohns.2006.12.022
- Yung M, Smith P, Hausler R, Martin C, Offeciers E, Pytel J, Skladzien J, Somers T, Ven de Heyning PL. International Common Otology Database: taste disturbance after stapes surgery. Otol Neurotol. 2008; 29:661-66. htths://doi org/10.1097/mao.0b013e3181778211
- Miuchi S, Sakagami M, Tsuzuki K, Noguchi K, Mishiro Y, Katsura H. Taste disturbance after stapes surgery–clinical and experimental study. Acta Otolaryngol Suppl. 2009; 562:71–78. htths://doi org/10.1080/00016480902915731
- Guder E, Böttcher A, Pau HW, Just T. Taste function after stapes surgery. Auris Nasus Larynx. 2012; 39:562-566. htths://doi org/10.1016/j.anl.2011.10.020
- Guinand N, Just T, Stow NW, Van HC, Landis BN. Cutting the chorda tympani: not just a matter of taste. J Laryngol Otol. 2010; 124:999-1002. htths://doi org/10.1017/s0022215110000733
- Chen JM, Bodmer D, Khetani JD, Lin VV. Tactile dysgeusia: a new clinical observation of middle ear and skull base surgery. 2008; 118:99-103. htths://doi org/10.1007/s00405-013-2420-5
- Mandel L. Hyposalivation after undergoing stapedectomy. J Am Dent Assoc. 2012; 143:39-42. htths://doi org/10.14219/jada.archive.2012.0016
- Kronenberg J., Migirov L, DaganT. Suprameatal approach: new surgical approach for cochlear implantation. J Laryngol Otol. 2001; 115:283–285. htths://doi org/10.1258/0022215011907451
- Orús Dotú C, Venegas Pizarro M del P, De Juan Beltrán J, De Juan Delago M. Cochlear reimplantation in the same ear: findings, peculiarities of the surgical technique and complications. Acta Otorrinolaringol Esp. 2010; 61:106. htths://doi org/10.1016/s2173-5735(10)70018-1
- Nevoux J, Loundon N, Leboulanger N, Roger G, Ducou Le Pointe H, Garabédian EN. Cochlear implant in the carotid canal. Case report and literature review. Int J Pediatr Otorhinolaryngol. 2010; 74:701-703. htths://doi org/10.1016/j.ijporl.2010.03.005
- Wagner JH, Basta D, Wagner F, Seidl RO, Ernst A, Todt I. Vestibular and taste disorders after bilateral cochlear implantation. Eur Arch Otorhinolaryngol. 2010; 267:1849-1854. htths://doi org/10.1007/s00 405-010-1320-1
- Mouzali A, Ouennoughi K, Haraoubia MS, Zemirli O, Triglia JM. Cochlear implant electrode array misplaced in Hyrtl's fissure. Int J Pediatr Otorhinolaryngol. 2011; 75:1459-1462. htths://doi org/10.1016/j.ijporl.2011.08.007
- Hara M, Takahashi H, Kanda Y. The usefulness of reconstructed 3D images in surgical planning for cochlear implantation in a malformed ear with an abnormal course of the facial nerve. Clin Exp Otorhinolaryngol. 2012; 5 (Suppl 1):48-52. htths://doi org/10.3342/ceo.2012.5.S1.S48
- Brito R, Monteiro TA, Leal AF, Tsuji RK, Pinna MH, Bento RF. Surgical complications in 550 consecutive cochlear implantation. Braz J Otorhinolaryngol. 2012; 78:80-85. htths://doi org/10.1590/s1808-86942012000300014
- Рзаев Р.М., Рзаев Р.Р. Эндоскопическая анатомия среднего уха (диссекционное исследование). Вестник оториноларингологии. 2017;82(5): 19-21.[Rzaev RM, Rzaev RR. The endoscopic anatomy of the middle ear (a dissection study). Vestnik otorinolaringologii, 2017;82(5): 19-21. (In Russ.)]. htths://doi org/10.17116/otorino201782519-21